Принципы противовоспалительной терапии. Противовоспалительная терапия диффузных заболеваний соединительной ткани - системная красная волчанка, системная склеродермия, ревматоидный артрит Задания для самоподготовки и уирс
В последние годы расширилось представление об индукторах воспаления аллергического генеза.
На исходном этапе наблюдаемая связь IgE с высокоаффинными Fc-рецепторами на мембране тучной клетки, базофилах, железистых образованиях предуготавливает запуск своеобразного воспалительного процесса.
Реализация его осуществляется при взаимодействии IgE с антигеном через рецептор Fab и экспрессией в связи с этим макрофагами, тучными клетками сложного каскада провоспалительных (ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-12, ту- морнекротический фактор а, интерфероны у) и противовоспалительных (ИЛ-4, ИЛ-10, ИЛ-13 и др.) цитокинов. Отдельные из них обладают преимущественно местным (ИЛ-4, ИЛ-5) или системным (ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-12) эффектом (И.С. Фрейллин, А.А. Тотолян, 1998; В.И. Немцов, Г.Б. Федосеев, 1998, и др.).
Провоспалительные цитокины направляют в очаг воспаления не только фагоцитирующие клетки, эозинофилы, но и Т-лим- фоциты, которые в свою очередь выбрасывают очередные каскады как провоспалительных, так и противовоспалительных цитокинов.
Наряду с этим в развитии воспаления в шоковом органе участвуют метаболиты арахидоновой кислоты, в частности различные лейкотриены (ЛТС4, JITD4, ЛТЕ4), усиливающие пролиферативные воспалительные, клеточные реакции (опосредованные эозинофилами), бронхиальную гиперреактивность, стимулирующие секрецию слизи, отек слизистой оболочки бронхов. Лейкотриены образуются разными путями: генерацией их тучными клетками, эозинофилами; стимуляцией синтеза их высокоокислительными радикалами, фактором активации тромбоцитов; активацией на фоне циклоксигеназного липоксигеназного пути синтеза просташандинов, особенно при непереносимости препаратов салициловой кислоты. Бронхоконстрикция под влиянием лейкотриенов существенно возрастает в присутствии различных метаболитов на фоне ПГБ2а, повышения продукции цГМФ с увеличением выхода Са2+ из саркоплазматического ретикулума (В.О. Самойлов, А.И. Колчев, 1998; Е.В. Евсюкова, 1998, и др.).
Неравновесность провоспалительных и противовоспалительных иммуноцитокинов при наличии индуктора воспаления - аллергена, триггерного воздействия макроэкономических факторов определяет более или менее благоприятное течение заболевания.
Используя современные технологии, с помощью противовоспалительных средств удается переломить течение заболевания, направить его в сторону сбалансированного гомеостаза.
В настоящее время предлагается большой перечень мероприятий, обеспечивающих проведение эффективной противовоспалительной терапии при аллергических заболеваниях (А.В. Емельянов, 1998):
Элиминация аллергена;
Специфическая иммунотерапия;
Лечение с использованием:
Мембраностабилизирующих препаратов (недокромил-на- трия, хромогликата натрия);
Антилейкотриеновых препаратов (зилеутона, зафирлукас- таидр.);
Антигистаминных препаратов (астемизола, акривастина, лоратадина, эбастина и др.);
Антибактериальных препаратов;
Метилксантина (теопэка, теотарда и др.);
Глюкокортикоидных препаратов.
Перечисленные средства нашли свое отражение в данном пособии.
Заслуживают отдельного изложения некоторые из них.
Метилксантины (производные теофиллина) используют в качестве бронходилататоров и средств, улучшающих микроциркуляцию в бассейне каротидных артерий, малого круга кровообращения, мочевьщелительной системы.
Полагают, что главным механизмом действия эуфиллина является блокада ФДЭ с последующим повышением цАМФ и чувствительности рг-адренорецепторов к катехоламинам.
Наряду с этим считают, что метилксантины при длительном использовании обладают противовоспалительным эффектом в результате: 1) блокады А(и стимуляции А2 из класса Р| пуриновых рецепторов, что также ведет к повышению цАМФ; 2) угнетения образования активного кислорода; 3) супрессии лейкотрие- на В4 и интерлейкина 2 (Nielson et al., 1988; Scordamagia, 1988).
К препаратам эуфиллина второго поколения с двукратным режимом дозирования относятся теопэк (таблетки по 100,200, 300 мг), теобиолонг (таблетки по 300 мг), теодур (таблетки по 100, 200,300 мг), вентакс (капсулы по 100,200,300 мг) и др., третьего поколения с однократным режимом дозирования - тео-24 (капсулы по 1200,1500 мг), эуфилонг (капсулы по 250,350,500 мг) и др. При назначении теофиллина следует осуществлять мониторинг за концентрацией его и в зависимости от нее дозировать препарат. Терапевтическая концентрация эуфиллина в плазме больного должна составлять 10-20 мкг/мл, при концентрации в плазме 20-30 мкг/мл возникают побочные реакции со стороны сердечно-сосудистой системы (тахикардия, нарушение ритма, возможна фибрилляция желудочков).
Как известно, в развитии воспалительных реакций в легких и бронхах при аллергии центральным и универсальным медиатором является высвобождение простаппандинов и лейкотриенов.
В связи с этим перспективно применение в лечении БА анти- лейкотриеновых препаратов. Среди них выделяют: I) прямые селективные ингибиторы 5-липоксигеназы (зилеутон и др.);
2) ингибиторы активирующего протеина мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886 и др.); 3) антагонисты рецепторов сульфидопептидных (С4, D4, Е4) лейкотриенов (зафирлукаст, монтелукаст, верлукаст и др.); 4) антагонисты рецепторов лейкотриенов В4 (И-75,-302 и др.). Как отмечает А.В. Емельянов (1998), среди них наиболее апробированы зилеутон (селективный и обратимый ингибитор 5-липоксигеназы) и зафирлукаст (монтелукаст, пранлукаст). Зилеутон предлагается в таблетках по 300 и 600 мг, препарат с коротким периодом полу- выведения, в связи с чем его назначают до 4 раз в сутки. Зафирлукаст (аколат) - таблетки по 20 и 40 мг, суточная доза (40- 160 мг) назначается в два приема, монтелукаст (сингуляр)-таблетки по 5 и 10 мг, принимают 1 раз в сутки, на ночь.
Клинические исследования показали, что аколат предупреждает развитие ранней и поздней реакции аллергии, развитие бронхоспазма, вызываемого JITD4, фактором активации тромбоцитов и провоцируемого холодным воздухом, физической нагрузкой, аспирином. Клиническая апробация антагонистов рецепторов лейюотриенов обнадеживает, они заняли свое место в лечении бронхиальной астмы не в качестве монотерапии, а в комплексной терапии (В.Л. Ковалева с соавт., 1998), так как существенно сокращают потребность больного в р2-агонистах, глюкокортикоидах и, по данным клеточного состава бронхиолярно-альвео- лярного лаважа, снижают интенсивность клеточных пролиферативных реакций (Holgate et al., 1996; Pauwels et al., 1995).
Среди перечисленных противовоспалительных препаратов более широкое распространение при лечении аллергических заболеваний получили кортикостероиды.
Глюкокортикоиды
Глюкокортикоиды в лечении аллергических болезней широко используются в качестве заместительной терапии (при глюкокортикоидной зависимости), как индукторы ремиссии (при сывороточной болезни, токсидермии), в качестве пульс-терапии (в больших дозах при астматическом статусе, анафилактическом шоке), в виде базовой терапии (современные ингаляционные глюкокортикоиды при бронхиальной астме). Однако применение глюкокортикоидов - это каждый раз отчаянная, вынужденная мера, которая требует углубленного анализа заболевания, прогноза, правильной оценки реальной эффективности неглюкокортикоидной терапии и, главное, определения мер, способствующих предупреждению последствий применения гормональных препаратов.
Эта проблема широко освещена в литературе (К. Абендрот, 1988; Б.И. Шмушкович, 1997; О. А. Суточникова, 1997; Б. С. Уте- шев, 1997; В. Шрейбер, 1987; Borumetal., Freedman, 1986; Michel, Delooz, 1989, и др.).
Глюкокортикоиды - биологически весьма активная часть гормонального гомеостаза, в продукции и саморегуляции которых главная роль отводится гипофизарно-надпочечниковой системе. В коре надпочечников синтезируется кортизон - биологически неактивное соединение, которое в печени превращается в активное - гидрокортизон (кортизол).
У взрослого человека за (утки вырабатывается 10-30 мг кортизола, в условиях стресса (различных перегрузок, травм, инфекций и др.) это количество может возрастать в 10 раз (до 250 мг). Потребность организма в кортизоле неравномерна в течение суток и зависит от активации обменно-ферментативных процес-
сов - основная его часть реализуется в дневной (особенно утром и в середине дня) период и лишь 1/10 - в ночное время.
Назначая глюкокортикоидные препараты, необходимо каждый раз предпринимать усилия, чтобы избежать возможных нежелательных реакций (табл. 7).
Табл. 7. Нежелательные реакции при применении глюкокортикоидов
 |  |
||
Системы, органы и физиологические эффекты
Проявление нежелательных реакций связано с продолжительностью глюкокортикоидной терапии, предрасположенностью к ним, наличием факторов риска-гипертензии, язвенной болезни желудка, избыточной массы тела, остеопороза. По времени развития они могут быть ранними или поздними (табл. 8).
| Табл. 8. Условия возникновения нежелательных реакций при использовании глюкокортикоидов (Boumpas et al., 1993) | |
| Условия возникновения | Нежелательные реакции |
| В начале лечения, избежать | Нарушение сна. |
| их появления невозможно | Эмоциональная лабильность. Повышение аппетита. Повышение массы тела |
| У больных, относящихся | Гипертензия. |
| к группам риска | Гипергликемия (вплоть до развития диабета). Ульцерогенный эффект. Угревая сыпь |
| При поддерживающей | Кушингоидный синдром. |
| или интенсивной терапии | Угнетение гилоталамо-гипофизарно- |
| (риск снижается при ис- | надпочечниковой системы. |
| пользовании минимальных | Инфекционные осложнения. |
| доз и щадящих режимов) | Остеонекроз. Миопатии. Нарушение заживления ран |
| Поздние реакции | Остеопороз. |
| (возможно, дозозависимые) | Атрофия кожи. Катаракта. Атеросклероз. Задержка роста. Жировое перерождение печени |
| Редкие и непредсказуемые | Психоз. |
| осложнения | Синдром псевдоопухоли мозга. Глаукома Эпидуральный липоматоз. Панкреатит |
Характеристика глюкокортикоидных препаратов. По времени полужизни в организме глюкокортикоиды условно делятся на короткоживущие: кортизон и гидрокортизон - 8-12 ч, предни- золон, метилпреднизолон - 12-36 ч; среднеживущие: триами- цинолон, параметазон - 24-48 ч; долгоживущие: бетаметазон, дексаметазон, беклометазон-36-54 ч.
Практически в той же последовательности нарастает глюкокортикоидная активность приведенных препаратов и угнетение гипоталамо-гипофизарно-надпочечниковой системы.
В связи с этим при длительной терапии необходимо отдать предпочтение короткоживущим препаратам (преднизолону или медролу), однако они обладают и большей минералокортикоид- ной активностью.
Глюкокортикоиды подразделяются на следующие группы:
Глюкокортикоиды, которые при приеме внутрь быстро всасываются в верхних отделах тонкого кишечника, создавая максимальную концентрацию в крови через 0,5-1,5 ч;
Сукцинаты, гемисукцинаты и фосфаты водорастворимых глюкокортикоидов, вводимых внутривенно, обладают быстрым и сравнительно кратковременным эффектом;
Ацетаты, ацетониды - мелкокристаллические суспензии глюкокортикоидов, нерастворимы в воде (предназначены для введения внутрь суставов, в суставные сумки, синовиальные влагалища, рубцы и реже внутримышечно), медленно всасываются с началом действия через 24-48 ч и общей продолжительностью до4нед.
Гидрокортизон как природный глюкокортикоид обладает в 4 раза более слабым противовоспалительным действием по сравнению с преднизолоном, как минералокортикоид превосходит его.
Применяется главным образом для заместительной терапии.
Форма выпуска:
Гидрокортизона ацетат, суспензия в ампулах - 25 мг/мл для внутримышечного введения, введения в суставные сумки идр.;
Гидрокортизона гемисукцинат, сухое вещество или раствор в ампулах - 100 и 500 мг (солу-кортеф, гидрокортизон-тева).
Преднизолон-синтетический глюкокортикоид.
Форма выпуска:
Таблетки-5,10,20 и 50 мг;
Преднизолона натрия фосфат, ампулы-30 мг/мл;
Преднизолона гемисукцинат (солю-декортин), порошок в ампулах-25,50 и 250 мг;
Преднизолона ацетат, суспензия в ампулах-25 и 50 мг.
Метштреднизопон-глюкокортикоидная активность на 20 % выше, чем у преднизолона, минимальный ульцерогенный побочный эффект. Обладает способностью подавлять перекисное окисление.
Форма выпуска:
Таблетки-4» 16,32 и 100 мг (медрол, метипред, урбазон);
Метилпреднизолона сукцинат, сухое вещество во флаконах -40,125,250,500 и 1000 мг (метипред, солу-медрол);
Метилпреднизолона ацетат, суспензия во флаконах - 40 мг (депо-медрол, метипред).
Триамцинолон-фторированный глюкокортикоид, действие на 20 % сильнее, чем у преднизолона.
Форма выпуска:
Таблетки-2,4,8 мг (полькортолон, кенакорт, берликорт);
Триамцинолона ацетонид, суспензия в ампулах-40 мг/мл (кеналог).
Дексаметазон-фторированный глюкокортикоид, обладает в 7 раз более сильным противовоспалительным действием, чем преднизалон, стимулирует синтез сурфактанта в альвеолах.
Форма выпуска:
Таблетки-0,5 и 1,5 мг (кортидекс, дексазон, даксин);
Дексаметазона фосфат натрия, ампулы - 4 мг/мл (дексазон, дексабене, сондекс).
Еетамстазон - фторированный глюкокортикоид, по силе и длительности действия близок к дексаметазону.
Форма выпуска:
Таблетки-0,5 мг (целестон);
Бетаметазона динатрия фосфат, ампулы - 3 мг/мл (целестон), может вводиться внутривенно, субконъюнктивально;
Бетаметазона ацетат, ампулы по 1 мл и флаконы по 5 мл- 3 мг/мл (целестон хронодозе);
Бетаметазона динатрия фосфат и дипропионат, ампулы по
1 мл суспензии, содержащие 7 мг бетаметазона, включающего
2 мг быстро всасывающегося фосфата и 5 мг медленно всасывающегося дипропионата (дипроспан, флостерон).
Применение глюкокортикоидов прн аллергических болезнях. Терапия глюкокортикоидами подразделяется на заместительную и противовоспалительную.
Заместительная терапия восполняет недостающий эндогенный кортизол на фоне недостаточности коры надпочечников. Препаратом выбора при такой терапии является гидрокортизон - средство, наиболее близкое к кортизолу.
Среди перечня нежелательных реакций при долговременной терапии глюкокортикоидами заслуживает внимания вторичная недостаточность надпочечников. Прогнозировать недостаточность надпочечников можно в следующих случаях:
1. При длительной поддерживающей терапии преднизалоном или медролом до 5 мг/сут, гидрокортизоном до 25 мг/сут угнетение гипоталамо-гипофизарно-надпочечниковой системы маловероятно.
При применении преднизолона, медрола в более высоких дозах (10 мг в сутки) более 10 дней может сформироваться недостаточность коры надпочечников, для восстановления которой требуется иногда 6 и более месяцев. Следует учитывать при этом и время приема преднизолона, медрола, например, вечерний прием в количестве 5 мг этих препаратов более опасен, чем 20 мг в утреннее время.
Можно с большой вероятностью прогнозировать наличие недостаточности надпочечников у тех лиц, которые лечились фторированными глюкокортикоидами длительное время (триам- цинолон, дексаметазон).
2. Признаки недостаточности коры надпочечников могут появиться у пациентов вскоре после отмены глюкокортикоидов - через 2-7 дней или через несколько месяцев после окончания курса лечения. Последняя ситуация может быть спровоцирована стрессовой нагрузкой (вследствие травмы, инфекции, операции, родов и др.). "
Недостаточность надпочечников (синдром отмены глюкокортикоидов) проявляется недомоганием, вялостью, быстрой утомляемостью, болью в мышцах, обострением основного заболевания. На этом фоне вероятность недостаточности надпочечников повышается при тахикардии, понижении артериального давления.
Чтобы предупредить недостаточность коры надпочечников, необходимо принять следующие меры.
Пациентам с прогнозируемой недостаточностью надпочечников во время стрессовой ситуации (травмы, операции, роды, повышение температуры тела) в профилактических целях показана заместительная терапия - внутримышечное введение гидрокортизона в дозе 25 мг/сут.
Если при этом наблюдаются клинические проявления недостаточности надпочечников, то доза гидрокортизона может повышаться до стрессовой потребности (250 мг/сут) в сочетании с капельным введением кровезаменителей до 1,5 л на фоне комплексной терапии.
Противовоспалительная терапия может проводиться в разных режимах как инициирующая (индукция ремиссии), долговременная, альтернативная, пульс-терапия, антиэметическая терапия, і нгаляционная долговременная терапия.
Противовоспалительный эффект глюкокортикоидов обусловлен рядом факторов.
1. Глюкокортикоиды, проникая через мембрану клеток, в цитоплазме связываются со специфическим рецептором, образуя активированные комплексы, стимулируют в ядре клетки образование информационной ДНК, обеспечивающей синтез различных регуляторных белков, включая и липокортин. Последний ингибирует фермент фосфолипазу А2, что приводит к снижению синтеза простагландинов, лейкотриенов, активаторов воспалительной реакции.
2. Глюкокортикоиды, стабилизируя мембраны клеток, внутриклеточных органелл, микросом, снижают проницаемость капилляров, тормозят миграцию нейтрофилов и макрофагов в очаг воспаления, угнетают пролиферацию фибробластов и синтез коллагена, снижают цитотоксическую активность Т-лимфоцитов, активацию Т-хелперов.
3. Глюкокортикоиды тормозят взаимодействие иммуноглобулинов с тучной клеткой, ингибируя высвобождение биологически активных веществ. Они также подавляют синтез «противовоспалительных» цитокинов ИЛ-1, ИЛ-6, ИЛ-8, фактора некроза опухолей.
Предлагаемые режимы противовоспалительной терапии позволяют максимально избегать побочных реакций.
Инициирующая терапия (индукцияремиссии) проводится медролом в расчете на оптимальный противовоспалительный эффект в дозе 0,8 мг метилпреднизолона на 1 кг массы тела в день, т.е. для пациента массой 60 кг потребуется прием 16 мг утром, в обед и вечером-всего 48 мг в сутки. В зависимости от клинической ситуации и предполагаемой регрессии заболевания суточная доза медрола может быть и меньшей.
В целом данный режим терапии направлен на переключение максимально выраженной воспалительной реакции на минимальную за максимально короткий период, охватывающий не более 7- 10 дней, а чаще 3-4 дня. Например, подобная терапия при лечении токсидермии может быть полностью закончена в эти же дни без специального режима отмены медрола.
Если невозможно полностью отменить медрол в течение 10 дней, переходят на режим долговременной терапии, проведение которой медролом позволяет более успешно избегать нежелательных реакций, чем, например, при лечении полькортолоном, дексаметазоном.
Долговременная противовоспалительная терапия. Суточная доза медрола практически остается такой же, как и при проведении инициирующей терапии, только распределяется оиа на два приема - утром и в обед.
Долговременная противовоспалительная терапия как вынужденная мера проводится при развитии эозинофильных инфильтратов, после купирования астматического статуса, после купирования токсидермии, развившейся на фоне рецидивирующей крапивницы.
Долговременная терапия может осуществляться в зависимости от ситуации в течение 2 недель или больше, и практически при стабилизации заболевания она проводится в альтернативном режиме.
Альтернативный режим. Сущность проводимого лечения заключается в том, что суточная доза медрола, предусмотренная при долговременной терапии, дается через день, т.е. лечение осуществляется в прерывистом режиме.
В ряде случаев при переходе на альтернативный режим суточную дозу медрола вначале назначают через день в половинной дозе. Например, в первый день 48 мг медрола, во второй - 24 мг и т.д. Затем, если ремиссия остается стойкой, половинная доза полностью снимается.
Альтернативный режим лечения предполагает наличие эндогенного кортизола, обеспечивающего компенсацию заболевания при подобном чередовании медрола через день.
Такое лечение может продолжаться до 3-4 нед. При стойкой ремиссии переходят на режим отмены медрола.
Для предупреждения недостаточности надпочечников-синдрома отмены глюкокортикоидов-в случаях проведения долговременной противовоспалительной терапии более 10 дней мед- ролом, преднизолоном в таблетках в дозе более 20-40 мг/сут снижать дозу этих препаратов у больных с наступившим клиническим благополучием нужно поэтапно:
а) если терапия преднизолоном, медролом продолжалась до 2 нед, то доза снижается по 4 мг каждую последующую неделю;
б) если терапия преднизолоном, медролом продолжалась более 2 нед, то доза снижается по 4 мг каждые две недели.
У больных бронхиальной астмой снижение дозы пероральных глюкокортикоидов на 4 мг возможно за одну неделю на фоне перехода на режим применения ингаляционных глюкокортикоидов.
Во избежание системного действия глюкокортикоидов, где это возможно, отдается предпочтение местному их применению и препаратам, которые могут всасываться в минимальных количествах (ингаляционные глюкокортикоиды - будезонид, флутика- зон; элоком при нанесении на кожные покровы).
Пульс-терапия - вынужденная мера при различных ургентних ситуациях. Может применяться в составе комплексной терапии при второй или третьей стадии астматического статуса, при выведении из анафилактического шока.
Пульс-терапия осуществляется в виде внутривенных инфузий солу-медрола, доза которого может составлять 0,5-1,0 г в сутки в течение 1-2-3 дней с последующей полной отменой препарата.
За больными при этом осуществляется постоянное наблюдение (наибольшую угрозу представляет изменение артериального давления и экстрасистолия). Пульс-терапия до 500 мг может осуществляться солу-медролом с осторожностью (при необходимости) лицам старше 50 лет.
Ингаляционные глюкокортикоиды при бронхиальной астме позволяют создать оптимальную противовоспалительную концентрацию в очаге воспаления и исключить системные нежелательные реакции при условии соблюдения правил их применения (с помощью спейсеров и полоскания полости рта после впрыскивания препарата).
Ингаляционные глюкокортикоиды не используются для купирования приступов удушья, они предназначаются для противовоспалительной, противоаллергической, антипролиферативной терапии при аллергических ринитах и бронхиальной астме (см.).
Беклометазон для ингаляций используется в дозе от 200 до 1600 мкг/сут, интраназально по 100 мкг 2 раза в день в каждую ноздрю.
Форма выпуска:
Дозированные аэрозоли - в одной дозе 50,100 (альдецин, бекотид, бекломет) и 250 мкг (беклокорт форте, беклофорт) бек- лометазона дипропионата;
Бекодиск - оригинальная форма выпуска беклометазона в виде пудры в разовых дозах 100 и 200 мкг, ингалируется с помощью дискхалера;
Дозированные аэрозоли для интраназального применения по 50 мкг беклометазона дипропионата (альдецин, беконазе, бек- ломет-назаль).
Флунизолид-фторированный глюкокортикоид, для ингаляций используется в дозе 1000 мкг/сут, интраназально-по 50 мкг в каждую ноздрю 2 раза в день.
Форма выпуска:
Флунизолид в виде дозированного аэрозоля со спейсе- ром - 250 мкг (ингакорт);
Дозированный ингалятор для интраназального применения, один вдох 25 мкг флунизолида (синтарис).
Будезонид - негалогенизированный глюкокортикоид.
Форма выпуска:
Будезонид в виде дозированного аэрозоля, один вдох 50 и 100 мкг (пульмикорт) и 200 мкг (бенакорт);
Будезонид в виде дозированного интраназального ингалятора, в одной дозе 50 мкг (ринокорт).
Флутиказон - препарат, имеющий высокий аффинитет к глюкокортикоидным рецепторам, превосходит будезонид в 2 раза.
Форма выпуска:
Фликсотид-дозированный аэрозоль, содержащий в одной дозе 25,50,125 и 250 мкг флутиказона;
Фликсоназе-дозированный интраназальный ингалятор, содержащий в одной дозе 50 мкг флутиказона.
Триамцинолон - фторированный глюкокортикоид.
Форма выпуска:
В виде дозированного аэрозоля со встроенным спейсером (азмакорт). Содержит в одной дозе 100 мкг триамцинолона аце- тонида;
Противовоспалительное действие кортикостероидов. Р.Дж. Флауэр, М.М. Дейл (R.J. Flower, M.M. Dale)
К противовоспалительным и десенсибилизирующим препаратам относятся, прежде всего, производные салициловой кислоты, пиразолона и гормональные препараты.
Натрия салицилат оказывает анальгезирующий, жаропонижающий и противовоспалительный эффект, ему свойственно также антигистаминное и антисептическое действие. Десенсибилизирующее влияние его наиболее отчетливо проявляется при ревматическом полиартрите (уменьшение и полное исчезновение внутрисуставного экссудата и периартикулярной отечности, устранение местного повышения температуры, быстрое купирование боли, полное восстановление функции пораженных суставов, нормализация температуры тела). Средняя суточная доза для взрослых в острой фазе болезни 8-12 г. Эта доза подбирается индивидуально в зависимости от терапевтического эффекта и переносимости препарата.
Достаточно эффективным и безопасным считается уровень салицилатов в крови до 35 мг%. При отсутствии заметного терапевтического эффекта в первые дни применения салицилатов дозу рекомендуется повысить.
При упорных формах заболевания с высокой температурой для повышения активности салициловой терапии применяют внутривенное введение 10% раствора натрия салицилата по 5-10 г на инъекцию 1-2 раза в день наряду с его приемом внутрь.
Существует единая точка зрения о времени назначения, способе применения и продолжительности лечения. Считают, что салицилаты следует назначать как можно раньше и в больших дозах (8--15 г в сутки). При стойком стихании острых явлений дозу салицилатов снижают до 4-б г в сутки до полной ликвидации клинических проявлений ревматического процесса.
При введении натрия салицилата в больших дозах возможны побочные явления (головокружение, сонливость, петехиальная сыпь на коже, диспепсические явления), в силу чего в последние годы натрия салицилат все чаще заменяют кислотой ацетилсалициловой, которая хорошо переносится как взрослыми, так и детьми. Она обладает хорошим противовоспалительным действием и гораздо реже вызывает побочные явления. Суточная доза 4- 6 г. При лечении ревматизма широко применяются препараты пиразо-лонового ряда (амидопирин, бута-дион и их аналоги). Амидопирин назначают по 0,5 г 4-6 раз в день. При этом необходимо систематически исследовать кровь, так как он может вызвать нейтропению, вплоть до агранулоцитоза. Субъективно амидопирин хорошо переносится, обладает сильным анальгезирующим действием.
Заменителем и производным амидопирина является анальгин, который применяют как per os (2- 3 г в день), так и внутримышечно (1-2 мл 25-50% раствора 2- 3 раза в день). Иногда уже через 15-30 мин после приема анальгина стихает боль в суставах. Однако по своему действию при ревматизме он все же несколько уступает амидопирину.
Производным пиразолонового ряда является бутадион (фенилбуазон, бутазолидин). Он обладает более энергичным антиревматическим действием по сравнению с салицилатами, а также более выраженным обезболивающим действием, ведет к быстрому снижению температуры тела и нормализации СОЭ, исчезновению симптомов ревматического перикардита, -смягчает или устраняет миогенные систолические шумы, а в отдельных случаях предупреждает развитие порока сердца. Более отчетливое влияние бутадиона отмечается при первичном ревмокардите, если лечение начато в первые 10-15 дней заболевания. При лечении бутадионом наступает более быстрое снижение повышенной проницаемости капилляров по сравнению с салицилатами. Однако у некоторых больных при лечении бутадионом наблюдаются побочные явления (снижение количества лейкоцитов, эритроцитов, тромбоцитов, гемоглобина, задержка жидкости и соли, гематурия, обострение язвенной болезни, диспепсические явления, кожная сыпь). Эти явления быстро проходят через несколько дней после отмены или снижения дозы препарата.
Бутадион назначают внутрь в порошках по 0,15 г 3-4 раза в день или внутримышечно (бутазолидин) по 2-3 мл 20% раствора ежедневно или по 5 мл через день. Противопоказан бутадион при язвенной болезни, лейкопении, анемии, сердечной декомпенсации, заболеваниях почек.
В настоящее время выпускают комбинированные препараты бутадиона (бутазолидина) с амидопирином — 1:1 (реопирин, пирабутол, иргапирин и др.). Форма выпуска — таблетки по 0,25 г и раствор. Применяют per os (3-4 таблетки в день), внутримышечно (2-3 мл ежедневно или по 5 мл 30% раствора через день). Показания и противопоказания такие же, как и у бутадиона.
Побочное действие производных пиразолона — нарушение водно-солевого обмена (задержка воды и натрия в организме с увеличением внеклеточной жидкости, уменьшением диуреза и значительным снижением эффективности мочегонных средств). Применение амидопирина и бутадиона может увеличивать степень недостаточности кровообращения, вплоть до приступов сердечной астмы. Поэтому при пороках сердца, более тяжелом течении ревмокардита и выраженной декомпенсации следует избегать назначения этих препаратов. Анальгин в меньшей степени способствует задержке в организме, воды и натрия.
При длительном применении производных пиразолона необходимо систематическое исследование крови (один раз в неделю), особенно при применении амидопирина, так как уже в самом начале его применения возможна лейкопения (вследствие повышенной чувствительности к препарату).
Продолжительность медикаментозной терапий при острой или подострой (активной) фазе болезни определяется состоянием реактивности организма и характером течения болезни, временем начала лечения, выполнением лечебного режима и ответной реакцией организма на проводимое лечение.
Длительность курса медикаментозного лечения устанавливается индивидуально для каждого больного. Лечение не должно прекращаться до исчезновения всех признаков активности ревматического процесса.
Продолжительность курса лечения короче при раннем его начале, в первые дни атаки, и дольше — при запоздалом — например, через месяц и позднее после начала заболевания. При рецидивирующих формах ревмокардита требуется длительное (3-5 месяцев) лечение, иногда повторным курсом в течение года, с применением различных антиревматических средств.
В последние годы при затяжном непрерывно рецидивирующем течении ревматизма рекомендуются препараты 4-аминохинолинового ряда — хингамин (делагил) и др. Лечебный эффект делагила (по 0,25- 0,5 г в день) проявляется через 3- 6 месяцев. При этом отмечается снижение экссудативных явлений и подавление продуктивных клеточных реакций, уменьшение высеваемости стрептококка из зева. При приеме делагила возможны побочные явления (гастралгии, лейкопения, кожная сыпь, зуд, снижение остроты и сужение полей зрения). Поэтому показано наблюдение окулиста и в случае необходимости — отмена препарата.
При ревматизме с выраженными нарушениями иммуногенеза, изменениями соединительной ткани, воспалительными реакциями, особенно аллергического характера, и т. д. показана гормональная терапия. Глюкокортикоиды обладают многосторонним действием. Наряду с угнетением образования плазматических и лимфоидно-ретикулярных клеток, в которых образуются антитела, они уменьшают продукцию антител и аутоантител, предупреждают связывание антител с производными мезенхимальной системы, снижая тем самым процессы дезорганизации соединительной ткани. Глюкокортикоиды также снижают миграцию нейтрофильных гранулоцитов и макрофагов, угнетают фагоцитоз, подавляют регенеративные процессы со стороны системы мононуклеарных фагоцитов (РЭС).
Угнетая выработку гиалуронидазы, подавляя продукцию гистамина, воздействуя на динамику кининов, стероиды снижают проницаемость капилляров тканей, играющих весьма важную роль в воспалительных и аллергических процессах. Кроме того, они через ферментные системы оказывают выраженное воздействие на функцию различных систем и органов, на обмен веществ организма. Наряду со снижением чувствительности тканей к аллергизирующим факторам, при применении стероидов повышаются чувствительность тканей к препаратам пиразолидинового ряда и эффективность препаратов, оказывающих патогенетическое действие. Несмотря на выраженное нарушение многих механизмов, стероиды, подавляя одни и усиливая другие процессы, способствуют выравниванию нарушенных реакций, тем самым способствуя сохранению гомеостаза.
Ред. проф. Г.И. Бурчинский
"Противовоспалительная терапия при ревматизме" — статья из раздела Ревматология
Дополнительная информация.
Противовоспалительная терапия
Как известно, воспаление является нормальной реакцией слизистой оболочки околоносовых пазух, направленной на уничтожение вирусов и бактерий. Это сложная комплексная местная сосудисто-тканевая защитно-приспособительная реакция целостного организма на действие патогенного раздражителя.
Основными компонентами воспаления являются:
альтерация с выделением медиаторов
сосудистая реакция с экссудацией
пролиферация
В ответ на это высвобождаются медиаторы воспаления, в свою очередь вызывающие пролиферацию лейкоцитов, активацию Т-лимфоцитов и дальнейшее усиление воспаления.
К основным медиаторам воспаления (а в настоящий момент их известно более 50) относят гистамин, простогландины, лейкотриены и цитокины. И простагландины и лейкотриены являются конечным продуктом метаболизма фосфолипадов клеточной мембраны. На первом этапе под воздействием фосфолипазы А 2 происходит метаболизм фосфолипидов клеточной мембраны до арахидоновой кислоты.
В дальнейшем циклооксигеназный путь метаболизма арахидоновой кислоты приводит к образованию простагландинов и тромбоксана, а липооксигеназный - к образованию лейкотриенов.
К провоспалительным цитокинам воспаления относятся интерлейкины (IL 1 , IL 3 , IL 4 , IL 5 , IL 6), фактор некроза опухолей (TNF α).
Результатом действия медиаторов воспаления становится усиление кровотока, изменение проницаемости сосудов, увеличение выхода клеток крови через сосудистую стенку с развитием отека . Кроме того респираторные агенты способны вызывать возрастание альфа-адренергической активности симпатических нервных окончаний, с чем связано увеличение образования вязкой слизи, и стимуляцию H 1 -гистаминовых рецепторов, приводящую к увеличению объема секрета за счет притока жидкости из-за повышенного поступления ионов натрия и хлора.
Таким образом, именно воспаление лежит в основе развития клинических симптомов и жалоб пациента с отитом.
Противовоспалительная терапия направлена в первую очередь на блокаду каскада медиаторных реакций, усиливающих воспалительную реакцию. Это ведет к купированию таких основных симптомов воспаления при острых синуситах как боль, отек, расширение сосудов слизистой оболочки околоносовых пазух, чрезмерная экссудация. Поэтому противовоспалительная терапия должна являться непременным звеном терапии острых синуситов (???).
В настоящее время различают два основных направления системной противовоспалительной терапии в целом - это противовоспалительные глюкокортикостероиды и нестероидные противовоспалительные средства.
Не отрицая большое значение глюкокортикостероидов в системной противовоспалительной терапии, следует указать на их полную непригодность в терапии острых синуситов (???). Благодаря своей способности к снижению антибактериальной активность фагоцитов и снижению секреции нейтральных протеаз глюкокортикостероиды ведут к снижению противоинфекционной защиты организма. Поэтому они не должны использоваться в комплексном лечении острого бактериального воспаления околоносовых пазух (???). В то же время, как местные, так и системные глюкокортикостероиды показали свою высокую эффективность в лечении аллергического воспаления (аллергические риниты и риносинуситы) и хронического полипозного риносинусита (за исключением полипозно-гнойной его формы) (???).
Нестероидные противовоспалительные средства (НПВС) ингибируют биосинтез простагландинов, угнетают активность циклооксигеназы, угнетают перекисное окисление липидов, влияют на кининовую систему. Все это делает их мощным средством в комплексном лечении острого бактериального воспаления околоносовых пазух (???)..
Нестероидные противовоспалительные средства по механизму своего действия делятся на две группы.
Первая группа - активные ингибиторы синтеза простагладинов (ибупрофен, флурбипрофен, диклофенак). Они наиболее активны при остром воспалении.
Вторая группа - сравнительно слабые ингибиторы синтеза простагландинов (индометацин, пироксикам, фенилбутозан). Эти препараты мало активны при остром воспалении, но весьма эффективны при хроническом.
Естественно, при лечении острых синуситов (???) предпочтение отдается препаратам первой группы.
В качестве противовоспалительной терапии неперфаративных острых отитов некоторые авторы предлагают местные глюкокортикостероидные препараты. Эффект от такого назначения может не всегда оправдать ожидания.
Комбинация местных глюкокортикостероидных препаратов и антибиотиков аминогликозиздного ряда прекрасно проявила себя при лечении острых наружных отитов. Это препараты гаразон (гентамицин + беклометозон), софрадекс (фрамецитина сульфа + дексаметазон), полидекса ушная (неомицин + полимиксин + дексаметазон). Такая комбинация позволяет не только эффективно ликвидировать микробную инфекцию, но и быстро купировать явления воспаления, благодаря эффективному действию местного кортикостероида. При остром среднем неперфоративном отите положительный эффект этих препаратов может быть обусловлен только противовоспалительным воздействием кортикостероидного компонента и, как следствие этого - частичным анальгезирующим эффектом. Потенциал же аминогликозидного антибиотика в данном случае остается неиспользованным. Поэтому при острых средних неперфоративных отитах целесообразнее использовать либо местные противовоспалительные препараты, либо противовоспалительные препараты в комбинации с анальгетиками локального действия.
Особняком от двух перечисленных групп системных противовоспалительных препартов стоит фенспирид (эреспал). Механизм действия фенспирида (эреспал) направлен непосредственно на метаболизм арахидоновой кислоты, путем блокирования транспорта ионов кальция, которые необходимы для активации фасфолипазы А 2 , что в свою очередь позволяет одновременно блокировать как образование простагландинов, так и лейкотриенов. В этом заключается важное преимущество фенспирида (эреспал) по сравнению с НПВП, влияющими только на циклооксигеназный путь метаболизма арахидоновой кислоты. НПВП не препятствуют накоплению таких сильных провоспалительных медиаторов, как лейкотриены, с чем и связаны их многие побочные эффекты. Важно отметить, что фенспирид (эреспал), не являясь стероидным противовоспалительным средством и обладая тропностью к слизистой оболочке дыхательного тракта, лишен неблагоприятных системных побочных эффектов ГКС.
Фенспирид (эреспал) снижает остроту воспалительного процесса не только посредством влияния на каскад арахидоновой кислоты, но также и за счет антагонизма в отношении гистамина посредством блокады Н 1 - рецепторов и ингибиции 1 – адренергических рецепторов, что способствует уменьшению гиперпродукции вязкого секрета в очаге воспаления. Кроме того, фенспирид (эреспал) оказывает ингибирующее действие на синтез и секрецию цитокинов, особенно на фактор некроза опухоли (TNF). Известно, что TNF усиливает цитотоксичность макрофагов, что с одной стороны, ведет к элиминации патогена, но с другой стороны, вызывает деструкцию тканей. Комплексный противовоспалительный механизм действия Эреспала позволяет быстрее нормализовать мукоциллиарный клиренс.
Эффективный контроль над воспалением способствует более быстрому разрешению основных клинических симптомов поражения уха.
Добавление фенспирида (эреспал) в схему лечения ЭСО позволяет быстрее добиться улучшения слуха, уменьшения чувства заложенности, снижения шума. Эффективность фенспирида (эреспала) подтверждена данными аудиометрии и тимпанометрии. Включение фенспирида (эреспал) в схему лечения пациентов с ЭСО сокращает сроки нормализации слуховых порогов по всей тон-шкале, а также сроки нормализации давления в полости среднего уха и восстановления подвижности барабанной перепонки (тимпанограмма типа А).
Таким образом, противовоспалительная терапия должна являться непременным звеном терапии острых отитов. По месту своего приложения фенспирид (эреспал) разработан специально для слизистых оболочек дыхательных путей, и поэтому при выборе средств системной противовоспалительной терапии острых отитов имеет преимущества перед другими противовоспалительными препаратами.
Системная антибиотикотерапия
Основным методом лечения ОСО, РОСО и ЗОСО является антимикробная терапия , причем первоначальный выбор антибиотика, как правило, бывает эмпирическим. Хотя не все формы ОСО требуют назначения антибиотиков, но лечение антибиотиками снижает риск развития мастоидита и других осложнений. Считается обязательным назначение антибиотиков во всех случаях ОСО у детей младше двух лет, а также пациентам с иммунодефицитными состояниями. Назначение антибиотиков необходимо при ЗОСО и РОСО.
Эмпирический выбор антибиотика должен учитывать спектр типичных возбудителей ОСО, ЗОСО и РОСО, каковыми являются пневмококк, гемофильная палочка, а в некоторых регионах – еще и моракселла . Оптимальным был бы выбор с учетом данных о региональной чувствительности предполагаемых возбудителей к антибиотикам, но в России эти данные не всегда достоверны и доступны лишь в отдельных регионах.
Чувствительность возбудителей ОСО к антибиотикам значительно варьирует в различных регионах. Общей тенденцией является нарастание резистентности пневмококков к пенициллину, макролидам и гемофильной палочки к ампициллину и амоксициллину. У пациентов, которые получали недавно курсы ампициллина, амоксициллина или пенициллина, значительно выше вероятность выделения микрофлоры, продуцирующей бета-лактамазы.
В Центральной части России у S.pneumoniae и H.influenzae, выделенных при ОСО, сохраняется высокая чувствительность к аминопенициллинам и цефалоспоринам: 97,0% штаммов S.pneumoniae чувствительны к амоксициллину, 100% - к к амоксициллину/клавуланату и цефуроксиму; 98% штаммов H.influenzae чувствительны к амоксициллину, 100% -к амоксициллину/клавуланату и цефуроксиму .
Основной проблемой является высокая резистентность пневмококка и гемофильной палочки к ко-тримоксазолу: резистентность отмечена у 35% штаммов S.pneumoniae и 18% H.influenzae .
Изложенное выше показывает, что стратегия использования нового фторхинолона левофлоксацина должна основываться на его применении не только в качестве альтернативного средства лечения внебольничных респираторных заболеваний и мочевых инфекций. Врач может предпочитать его в таких конкретных ситуациях как пожилой возраст больного, недавно проведенные курсы антибиотикотерапии, алкоголизм, нарушения иммунитета, недавняя госпитализация, лечение в условиях дневного стационара и некоторых других случаях, когда фармакодинамические и фармакокинетические преимущества левофлоксацина способны сыграть решающую роль в исходе заболевания важно осуществлять реалистичную сравнительную фармакоэкономическую оценку различных противомикробных средств с учетом всех факторов .
Очевидно также, что в перспективе (после детальных исследований) перечень показаний для левофлоксацина может расшириться за счет других нозокомиальных инфекций, требующих применения парентеральных бактерицидных антибактериальных средств широкого спектра. Поэтому в ряде публикаций последних двух лет высказываются предположения по применению левофлоксацина в схеме лечения острых средних гнойных отитов средний тяжести и тяжелых как препарата, альтернативного традиционным бета-лактамным антибиотикам .
Учитывая широкое распространение ятрогенной антибиотиковой тугоухости в России следует строго запретить назначение любых антибиотиков аминогликозидного ряда при острых средних отитах. Воспалительный процесс в барабанной полости способствует проникновению аминогикозидов в жидкости внутреннего уха и токсическому поражению нейросенсорных клеток.
Секретолитическая терапия
Как уже было показано, в этиопатоненезе острых средних отитов ключевую роль играет дисфункция слуховой трубы. Главным образом в терапии отитов внимание обращает на восстановление воздухопроводящей функции слуховой трубы - адренализация устья, катетеризация, вазоконстрикторные препараты.
Но не менее важной является дренажная функция слуховой трубы. Благодаря согласованным колебаниям ресничек мерцательного эпителия, выстилающих просвет слуховой трубы, происходит эвакуация патологического содержимого из барабанной полости. При отеке слизистой оболочки трубы функции эта полностью утрачивается. К тому же, густой вязкий секрет, заполняющий барабанную полость, с трудом поддается эвакуации.
Аналогичные процессы происходят в околоносовых пазухах при острых синуситах и с успехом купируются с помощью муколитической, секретомоторной и секретолитической терапии. В комплексной же терапии недостаточно разработанным.
Важное значение в лечении синуситов имеют расплавление или размягчение и разжижение вязкого, густого секрета. Прием медикаментов с дифференцированным действием на продукцию секрета, уменьшение вязкости слизи и функцию ресничек позволяет реактивировать нарушенное мукоцилиарное очищение. Лекарственные средства, оказывающие подобный терапевтический эффект, объединяют в группы муколитических, секретомоторных и секретолитических препаратов .
Муколитические препараты изменяют физико-химические свойства секрета путем уменьшения его вязкости. С этой целью применяются смачиватели, снижающие поверхностное натяжение, или ферменты, вызывающие разрыв дисульфидных связей.
К секретомоторным препаратам относят лекарственные средства, которые через различные механизмы, в основном путем усиления моторной активности мерцательного эпителия, повышают эффективность мукоцилиарного очищения. Типичными представителями этой группы являются известные как бронхорасширяющие средства стимуляторы b2-адренорецепторов. Секретомоторным действием обладают также теофиллин, бензиламины и прежде всего эфирные масла.
Секретолитические препараты являются лекарственными средствами, улучшающими эвакуацию слизи путем изменения характера секреции. Эфирные масла растительного происхождения, экстракты различных растений, производные креозота (гваякол) и синтетические бензиламины, бромгексин и амброксол оказывают секретолитический эффект через механизм усиления секреции бронхиальных желез. Сложность фармакологической оценки муколитических, секретолитических и секретомоторных препаратов заключается в том, что до сих пор не имеется надежного метода экспериментального подтверждения их эффективности.
Одним из немногих препаратов этой группы, применяющийся в лечении острых средних отитов является сунупрет.
В последние годы расширилось представление об индукторах воспаления аллергического генеза.
На исходном этапе наблюдаемая связь IgE с высокоаффинными Fc-рецепторами на мембране тучной клетки, базофилах, железистых образованиях предуготавливает запуск своеобразного воспалительного процесса. Реализация его осуществляется при взаимодействии IgE с антигеном через рецептор Fab и экспрессией в связи с этим макрофагами, тучными клетками сложного каскада провоспалительных (ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-12, ту- морнекротический фактор а, интерфероны у) и противовоспалительных (ИЛ-4, ИЛ-10, ИЛ-13 и др.) цитокинов. Отдельные из них обладают преимущественно местным (ИЛ-4, ИЛ-5) или системным (ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-12) эффектом (И.С. Фрейллин, А.А. Тотолян, 1998; В.И. Немцов, Г.Б. Федосеев, 1998, и др.).
Провоспалительные цитокины направляют в очаг воспаления не только фагоцитирующие клетки, эозинофилы, но и Т-лим-
фоциты, которые в свою очередь выбрасывают очередные каскады как провоспалительных, так и противовоспалительных цитокинов.
Наряду с этим в развитии воспаления в шоковом органе участвуют метаботиты арахидоновой кислоты, в частности различные лейкотриены (ЛТС4, JITD4, JITE4), усиливающие пролиферативные воспалительные, клеточные реакции (опосредованные эозинофилами), бронхиальную гиперреактивность, стимулирующие секрецию слизи, отек слизистой оболочки бронхов. Лейкотриены образуются разными путями: генерацией их тучными клетками, эозинофилами; стимуляцией синтеза их высокоокислительными радикалами, фактором активации тромбоцитов; активацией на фоне циклоксигеназного липоксигеназного пути синтеза просташандинов, особенно при непереносимости препаратов салициловой кислоты. Бронхоконстрикция под влиянием лейкотриенов существенно возрастает в присутствии различных метаболитов на фоне nrF2a, повышения продукции цГМФ с увеличением выхода Са2+ из саркоплазматического ретикулума (В.О. Самойлов, А.И. Колчев, 1998; Е.В. Евсюкова, 1998, и др.).
Неравновесность провоспалительных и противовоспалительных иммуноцитокинов при наличии индуктора воспаления - аллергена, триггерного воздействия макроэкологических факторов определяет более или менее благоприятное течение заболевания.
Используя современные технологии, с помощью противовоспалительных средств удается переломить течение заболевания, направить его в сторону сбалансированного гомеостаза.
В настоящее время предлагается большой перечень мероприятий, обеспечивающих проведение эффективной противовоспалительной терапии при аллергических заболеваниях (А.В. Емельянов, 1998):
- элиминация аллергена;
- специфическая иммунотерапия;
- лечение с использованием:
- мембраностабилизирующих препаратов (недокромил-на- трия, хромогликага натрия);
- антигистаминных препаратов (астемизола, акривастина, лоратадина, эбастина и др.);
- антибактериальных препаратов;
- ппококортикоидных препаратов.
Заслуживают отдельного изложения некоторые из них.
Метилксантины (производные теофиллина) используют в качестве бронходилататоров и средств, улучшающих микроциркуляцию в бассейне каротидных артерий, малого круга кровообращения, мочевыделительной системы.
Полагают, что главным механизмом действия эуфиллина является блокада ФДЭ с последующим повышением цАМФ и чувствительности р2-адренорецепторов к катехоламинам.
Наряду с этим считают, что метилксантины при длительном использовании обладают противовоспалительным эффектом в результате: 1) блокады А(и стимуляции А2 из класса Р| пуриновых рецепторов, что также ведет к повышению цАМФ; 2) угнетения образования активного кислорода; 3) супрессии лейкотрие- на В4 и интерлейкина 2 (Nielson et al., 1988; Scordamagia, 1988).
К препаратам эуфиллина второго поколения с двукратным режимом дозирования относятся теопэк (таблетки по 100,200, 300 мг), теобиолонг (таблетки по 300 мг), теодур (таблетки по 100, 200,300 мг), вентакс (капсулы по 100,200,300 мг) и др., третьего поколения с однократным режимом дозирования - тео-24 (капсулы по 1200,1500 мг), эуфилонг (капсулы по 250,350,500 мг) и др. При назначении теофиллина следует осуществлять мониторинг за концентрацией его и в зависимости от нее дозировать препарат. Терапевтическая концентрация эуфиллина в плазме больного должна составлять 10-20 мкг/мл, при концентрации в плазме 20-30 мкг/мл возникают побочные реакции со стороны сердечно-сосудистой системы (тахикардия, нарушение ритма, возможна фибрилляция желудочков).
Как известно, в развитии воспалительных реакций в легких и бронхах при аллергии центральным и универсальным медиатором является высвобождение простаппандинов и лейкотриенов.
В связи с этим перспективно применение в лечении БА анти- лейкотриеновых препаратов. Среди них выделяют: I) прямые селективные ингибиторы 5-липоксигеназы (зилеутон и др.); 2) ингибиторы активирующего протеина мембраносвязанного белка с арахидоновой кислотой (МК-0591, МК-886 и др.); 3) антагонисты рецепторов сульфидопептидных (С4, D4, Е4) лейкотриенов (зафирлукаст, монтелукаст, верлукаст и др.); 4) антагонисты рецепторов лейкотриенов В4 (И-75,-302 и др.). Как отмечает
А.В. Емельянов (1998), среди них наиболее апробированы зилеутон (селективный и обратимый ингибитор 5-липоксигеназы) и зафирлукаст (монтелукаст, пранлукаст). Зилеутон предлагается в таблетках по 300 и 600 мг, препарат с коротким периодом полу- выведения, в связи с чем его назначают до 4 раз в сутки. Зафирлукаст (аколат) - таблетки по 20 и 40 мг, суточная доза (40- 160 мг) назначается в два приема, монтелукаст (сингуляр)-таблетки по 5 и 10 мг, принимают 1 раз в сутки, на ночь.
Клинические исследования показали, что аколат предупреждает развитие ранней и поздней реакции аллергии, развитие бронхоспазма, вызываемого JITD4, фактором активации тромбоцитов и провоцируемого холодным воздухом, физической нагрузкой, аспирином. Клиническая апробация антагонистов рецепторов лейюотриенов обнадеживает, они заняли свое место в лечении бронхиальной астмы не в качестве монотерапии, а в комплексной терапии (B.J1. Ковалева с соавт., 1998), так как существенно сокращают потребность больного в р2-агонистах, глюкокорти- коидах и, по данным клеточного состава бронхиолярно-альвео- лярного лаважа, снижают интенсивность клеточных пролиферативных реакций (Holgate et al., 1996; Pauwels et al., 1995).
Среди перечисленных противовоспалительных препаратов более широкое распространение при лечении аллергических заболеваний получили кортикостероиды.
Catad_tema Бронхиальная астма и ХОБЛ - статьи
Противовоспалительная терапия хронической обструктивной болезни легких: настоящее и будущее
С.Н. Авдеев, ФБГУ «НИИ пульмонологии» ФМБА России
Сегодня хроническая обструктивная болезнь легких представляет собой значительную экономическую и социальную проблему и является единственной болезнью, при которой смертность продолжает увеличиваться . По данным ряда недавно выполненных исследований, распространенность хронической обструктивной болезни легких в мире у людей старше 40 лет составляет 10,1% (11,8% у мужчин и 8,5% у женщин) .
Ключевые слова:
хроническая обструктивная болезнь легких, Т-лимфоциты, мокрота, рофлумиласт
Значение воспаления в патогенезе хобл
Хроническая обструктивная болезнь легких (ХОБЛ) -заболевание, характеризующееся ограничением воздушного потока с развитием не полностью обратимой бронхиальной обструкции; ограничение воздушного потока прогрессирует и связано с усиленным патологическим воспалительным ответом дыхательных путей на повреждающие частицы или газы . Курение и другие ингаляционные ирританты инициируют развитие воспалительного ответа в дыхательных путях и легочной паренхиме. Воспаление у «здоровых» курильщиков по составу клеточных элементов, медиаторов и протеаз очень похоже на воспаление у пациентов с ХОБЛ, но менее выражено . Поэтому полагают, что воспаление в дыхательных путях и паренхиме при ХОБЛ представляет собой усиленный хронический воспалительный ответ на ирританты (такие как табачный дым) . Механизм такого усиления или амплификации пока остается до конца не изученным, он может детерминироваться генетическими факторами , латентными вирусными инфекциями и нарушением активности деацетилазы гистонов .
Основное место локализации характерной для ХОБЛ дыхательной обструкции - это малые дыхательные пути (ЦП) диаметром менее 2 мм . Но картина воспалительного инфильтрата в крупных и малых дыхательных путях, а также в легочной паренхиме и стенке легочных сосудов в целом довольно сходная . Данное воспаление может разрешаться или приводить к фиброзу, протеолизу и ремоделированию. Hogg и колл. показали, что по мере возрастания тяжести ХОБЛ происходит прогрессирующее утолщение стенки бронха, вызванное аккумуляцией клеток воспаления, а также накопление избытка слизи в просвете бронха . Воспалительный инфильтрат состоит из нейтрофилов, макрофагов и Т-лимфоцитов (CD4 + и CD8 +) и других клеток (рис. 1).
Рисунок 1.
Патогенез ХОБЛ (Martin et al. Int J COPD 2013)
Одну из ведущих ролей в воспалении при ХОБЛ играют нейтрофилы. O"Donnell et al. показали, что число нейтрофилов в индуцированной мокроте хорошо коррелирует с тяжестью поражения малых ДП по данным КТВР (отношение средних плотностей легких во время выдоха и вдоха), но не с тяжестью эмфиземы . Нейтрофильное воспаление ДП связано с гиперпродукцией секрета в проводящих ДП .
У пациентов с ХОБЛ обнаруживают повышенное содержание макрофагов в ДП, и эти макрофаги могут демонстрировать различные фенотипические черты . Frankenberger и колл. показали, что среди макрофагов, изолированных из индуцированной мокроты пациентов ХОБЛ, 46% были малыми макрофагами, в то время как у здоровых добровольцев обнаруживали лишь 1% малых макрофагов .
Повышенное содержание Т-лимфоцитов при ХОБЛ обнаруживают в проксимальных ДП, в малых ДП и в альвеолах . Saetta и колл. выявили у пациентов с ХОБЛ в эпителии малых ДП CD8+ Т-лимфоциты, экспрессирующие CXCR3, хемокиновый рецептор и его лиганд-интерферон-индуцированный протеин 10/CXCL10 . Аккумуляция активированных CD8+ Т-лимфоцитов в дистальных ДП у больных ХОБЛ была ассоциирована с различными структурными изменениями, что говорит о важной роли этих клеток в патогенезе ХОБЛ .
Пока недостаточно изучена роль в воспалительной реакции ДП таких клеток, как тучные клетки и эозинофилы. Grashoff et al. показали значительное повышение числа интраэпителиальных тучных клеток у пациентов с ХОБЛ, что не исключает их роль в патогенезе структурных изменений, приводящих к бронхиальной обструкции . Эозинофильную инфильтрацию проксимальных ДП обнаруживают у больных ХОБЛ во время обострений , особенно вызванных вирусной инфекцией , и в т. ч. у больных ХОБЛ с хроническим кашлем и выраженной продукцией мокроты .
Анализ бронхиальных биопсий и индуцированной мокроты у бросивших курить пациентов демонстрирует схожий воспалительный процесс, что предполагает персистенцию воспаления даже после прекращения действия ингаляционных ирритантов (курения) .
С учетом такой важной роли воспаления ДП в патогенезе ХОБЛ неудивительно, что противовоспалительной терапии при данном заболевании сегодня уделяют огромное внимание. К числу противовоспалительных препаратов для терапии ХОБЛ сегодня относятся ингаляционные глюкокортикостероиды (ИГКС), а новые перспективы противовоспалительной терапии ХОБЛ связывают с препаратами из класса ингибиторов фосфодиэстеразы-4 (рофлумиласт) , с новыми макролидами и статинами .
Ингаляционные глюкокортикостероиды
Согласно современным руководствам, терапия ИГКС рекомендована больным с тяжелыми и крайне тяжелыми стадиями ХОБЛ при наличии частых обострений; терапия ИГКС добавляется к терапии длительно действующими (ДД) бронходилататорами . Важное место среди лекарственных средств (ЛС), использующихся для длительной поддерживающей терапии ХОБЛ, занимают комбинированные препараты - ИГКС плюс длительно действующие β2-агонисты (ДДБА) . Так же как и ИГКС, комбинированная терапия ИГКС/ (ДДБА) в настоящее время рекомендована для применения больным с III-IV стадиями (по классификации GOLD) и с частыми обострениями . Научное обоснование комбинации ИГКС/ДДБА вытекает из комплементарных эффектов препаратов: ИГКС повышают экспрессию гена β2-рецептора и уменьшают потенциал для развития десенситизации β2-рецептора, в то время как β2-агонисты активируют неактивные ГКС-рецепторы, делая их более чувствительными для стероидзависимой активации .
Данные об эффективности ИГКС у больных ХОБЛ довольно противоречивы. В некоторых краткосрочных исследованиях терапия ИГКС не приводила к значимой модификации воспалительной реакции у больных ХОБЛ (рис. 2) . Однако в ряде работ показано, что терапия ИГКС в сочетании с ДДБА и без них может не оказать влияния на маркеры воспаления в мокроте, но может повлиять на воспаления в стенке бронха по данным биопсий . Краткосрочная терапия ИГКС (в течение 2-3 месяцев) у больных со среднетяжелой ХОБЛ приводила к уменьшению числа тучных клеток, не влияла на СD8 + -лимфоциты, нейтрофилы и макрофаги . Комбинированная терапия ИГКС/ДДБА в течение 3 месяцев оказалась более эффективной по влиянию на бронхиальное воспаление по сравнению с плацебо и, в сравнении с ИГКС, приводила к снижению числа СD8 + -клеток и макрофагов . По данным исследования GLUCOLD, терапия флутиказоном в течение 30 месяцев приводила к стойкому уменьшению числа Т-лимфоцитов и тучных клеток в слизистой бронхов, однако после прекращения терапии ИГКС в течение 6 месяцев вновь наблюдалось усиление воспалительной реакции , т. е. данные этого исследования указывают на то, что противовоспалительные эффекты терапии ИГКС не «закрепляются» надолго .

Рисунок 2.
Влияние терапии на ИГКС и ИГКС/ДДБА на клетки воспаления в дыхательных путях больных ХОБЛ (по данным бронхобиопсии) (Bourbeau J. et al. Thorax 2007)
Jen и колл. провели метаанализ на основе 8 рандомизированных исследований, посвященных изучению эффектов ИГКС на маркеры воспаления дыхательных путей по данным бронхоальвеолярного лаважа (БАЛ) (n = 102) и данным эндобронхиальных биопсий (n = 309) . По сравнению с пациентами контрольной группы, у больных, принимавших ИГКС, стандартизованное среднее различие (ССР) по числу нейтрофилов в жидкости БАЛ составило -0,64 ед. (р = 0,003). ИГКС также снижали число лимфоцитов в жидкости БАЛ (ССР -0,64 ед., р = 0,01). Терапия ИГКС не оказывала никакого эффекта на эозинофилы БАЛ, но приводила к повышению числа альвеолярных макрофагов (ССР 0,68 ед., р = 0,002). ИГКС не влияли на число нейтрофилов в бронхиальных биоптатах (ССР 0,61 ед., р = 0,10). Однако терапия ИГКС приводила к достоверному снижению числа CD8-лимфоцитов (ССР -0,66 ед., р = 0,002) и СD4-лимфоцитов (ССР -0,52 ед., р = 0,001) в препаратах эндобронхиальных биопсий. ИГКС не оказывали никакого влияния на число тканевых CD68-макрофагов и эозинофилов. Основные результаты метаанализа схематично представлены в таблице .
Таблица.
Влияние терапии ИГКС на маркеры воспаления дыхательных путей по данным БАЛ (n = 102) и данным эндобронхиальных биопсий (n = 309)
Менее выраженная эффективность ИГКС при ХОБЛ, по сравнению с бронхиальной астмой, может быть объяснена с позиции снижения экспрессии и активности одного из ключевых ядерных ферментов - деацетилазы гистонов-2 (HDAC-2), который необходим для «выключения» активированных воспалительных генов . Снижение активности HDAC-2 и относительная резистентность воспаления при ХОБЛ к ИГКС являются следствием выраженного окислительного и нитративного стресса в дыхательных путях пациентов ХОБЛ .
Согласно ряду исследований регулярная противовоспалительная терапия ИГКС у больных ХОБЛ улучшает симптомы, функциональные показатели, качество жизни и снижает число обострений у пациентов с ХОБЛ . Отмена ИГКС (под прикрытием ДДБА) приводит к снижению ОФВ 1 , нарастанию симптомов, ухудшению качества жизни и повышению числа обострений .
В одном из самых масштабных исследований, проведенных в последнее время (наблюдение за 6 000 больными ХОБЛ на протяжении 3 лет) - TOwards a Revolution in COPD Health (TORCH), было продемонстрировано, что длительная поддерживающая терапия ИГКС (флутиказоном), ДДБА (салметеролом) и ИГКС/ДДБА (салметеролом/флутиказоном) приводит к замедлению скорости снижения OФB1 на 13,13 и 16 мл/год соответственно . Согласно результатам недавно выполненного метаанализа, основанного на 27 исследованиях (30 495 пациентов с ХОБЛ), комбинированная терапия ИГКС/ДЦБА приводит к снижению общей летальности больных на 20% (ОР 0,80; р = 0,005) .
При терапии больных ХОБЛ необходимо помнить о возможных нежелательных реакциях со стороны ИГКС. По данным когортных исследований, применение ИГКС сопровождается определенным риском развития остеопороза и катаракты . Пневмония чаще осложняет терапию ИГКС и ИГКС/ДЦБА по сравнению с ЦЦ бронхолитиками и плацебо , но в то же время на фоне терапии ИГКС/ДЦБА отмечен более низкий уровень летальности и меньшее число обострений ХОБЛ. По данным крупного когортного исследования, терапия ИГКС была ассоциирована с повышением на 34% риска развития сахарного диабета и риском прогрессирования диабета .
Ингибиторы фосфодиэстеразы-4
Ингибиторы фосфодиэстеразы-4 (ФДЭ-4) пока представлены всего одним препаратом - рофлумиластом, который оказывает разнообразное противовоспалительное действие и специфически влияет на основные механизмы воспаления при ХОБЛ. Практически все клетки, участвующие в воспалении дыхательных путей при ХОБЛ, содержат изофермент ФДЭ-4 .
Противовоспалительная активность рофлумиласта в модели астмы на мышах и in vitro в легочных фибробластах эмбриона человека проявлялась в уменьшении ремоделирования дыхательных путей и в антифибротическом эффекте, сравнимом с эффектом дексаметазона при хроническом аллергическом воспалении . В животных моделях ХОБЛ рофлумиласт снижал число нейтрофилов в БАЛ и гиперсекрецию слизи, однако при хроническом воздействии табачного дыма противовоспалительный эффект рофлумиласта проявлялся только при высоких дозах препарата и заключался в уменьшении макрофагального воспаления и уменьшении площади эмфиземы без влияния на гиперплазию бокаловидных клеток . Данные, полученные на различных животных моделях, свидетельствуют о способности рофлумиласта уменьшать содержание нейтрофилов дыхательных путей, но в то же время - о неэффективности таких средств, как метилпреднизолон и дексаметазон .
Grootendorst и колл. в рандомизированном плацебо-контролируемом перекрестном исследовании изучали эффекты рофлумиласта на цитологический профиль индуцированной мокроты у больных ХОБЛ . Терапия рофлумиластом в течение 4 недель привела к улучшению функциональных показателей, а также снижению количества воспалительных клеток в мокроте, таких как нейтрофилы (рис. 3), лимфоциты и эозинофилы . Кроме того, на фоне терапии рофлумиластом отмечено уменьшение концентрации воспалительных маркеров - нейтрофильной эластазы, IL-8, эозинофильного катионного белка и α2-макроглобулина - маркера микроваскулярной проницаемости .

Рисунок 3.
Рофлумиласт уменьшает уровни маркеров воспаления в мокроте больных ХОБЛ (Grootendorst et al. Thorax 2007)
Клиническая эффективность рофлумиласта у пациентов с ХОБЛ среднетяжелого и тяжелого течения была продемонстрирована в серии крупных рандомизированных плацебо-контролируемых исследований. Рофлумиласт не обладает прямым бронхорасширяющим действием, но благодаря своим противовоспалительным эффектам способен улучшить функциональные показатели у пациентов с ХОБЛ . В исследовании Rabe и колл. рофлумиласт улучшил постбронходилатационный OФB1 на 74 мл в минимальной (250 мг/сут) и на 97 мл в максимальной дозировках (500 мг/сут) по сравнению с плацебо .
В двух исследованиях среднее число тяжелых и среднетяжелых обострений ХОБЛ на одного пациента в год значительно снизилось у больных, получавших рофлумиласт, по сравнению с плацебо: отношение риска (ОР; 0,83) независимо от одновременного приема ДДБА .
Rennard и колл. выполнили совокупный post-hoc-анализ исследований, изучавших эффективность рофлумиласта у пациентов с тяжелой и очень тяжелой ХОБЛ (стадии III и IV по классификации GOLD), и показали значительное снижение числа обострений ХОБЛ в подгруппе больных с бронхитическим вариантом ХОБЛ (т. е. с хроническим кашлем и продукцией мокроты) - на 26,2% (р = 0,001), в то время как в целом по группе ХОБЛ снижение числа обострений составило 14,3% (р = 0,026) (рис. 4) . Bateman и колл. на основе двух других исследований проанализировали влияние рофлумиласта на число обострений у пациентов с ХОБЛ с частыми (≥ 2 в год) и нечастыми (< 2 в год) обострениями (рис. 5) . У больных с нечастыми обострениями терапия рофлумиластом приводила к достоверному снижению числа обострений по сравнению с плацебо на 16,5% (р = 0,006). Но у больных с частыми обострениями различие с плацебо оказалось еще более выраженным - 22,3% (р = 0,002).

Рисунок 4.
Терапия рофлумиластом приводит к наибольшему снижению числа обострений у больных с бронхитическим типом ХОБЛ

Рисунок 5.
Терапия рофлумиластом приводит к наибольшему снижению числа обострений у больных ХОБЛ с частыми обострениями
В соответствии с современными рекомендациями GOLD рофлумиласт рассматривается как терапия, назначаемая дополнительно к приему комбинации ИГКС и ДДБА или к приему ДД антихолинергических препаратов у пациентов с выраженными симптомами, тяжелой или очень тяжелой бронхиальной обструкцией и высоким риском обострений .
Из наиболее частых нежелательных явлений можно отметить диарею, тошноту, снижение аппетита, снижение массы тела и головную боль . Большинство нежелательных явлений носили легкий и умеренный характер. Нежелательные явления при приеме рофлумиласта появлялись чаще всего в первые недели приема препарата и разрешались в ходе его дальнейшего приема . У пациентов ХОБЛ, получавших терапию рофлумиластом, было отмечено более частое, по сравнению с плацебо, снижение массы тела. После отмены рофлумиласта масса тела большинства пациентов восстановилась в течение 3 месяцев.
Длительная терапия макролидами
В настоящее время накапливается все больше и больше данных (причем не только в экспериментальных, но и в клинических исследованиях) о том, что макролидные антибиотики обладают важными иммуномодулирующими и противовоспалительными свойствами, которые могут быть использованы для контроля воспаления при хронических заболеваниях дыхательных путей .
Противовоспалительные свойства макролидов тесно связаны с их структурным строением - иммуномодулирующая активность была выявлена только у 14-членных (эритромицин, кларитромицин и ротроксимицин) и 15-членных макролидов (азитромицин), но не у 16-членных макролидов (спирамицин, джозамицин). Сегодня в клинической практике для терапии хронических воспалительных бронхолегочных заболевании используются преимущественно макролиды нового поколения - азитромицин или кларитромицин .
Потенциальными механизмами действия макролидов при хронических воспалительных бронхолегочных заболеваниях могут быть ингибиторные эффекты на секрецию в дыхательных путях , на аккумуляцию нейтрофилов и лимфоцитов в дыхательных путях и антипролиферативное воздействие на активноделящиеся клетки (рис. 6) .

Рисунок 6.
Потенциальные механизмы действия макролидов при хронических воспалительных бронхолегочных заболеваниях
Эффективность терапии макролидами воспалительных заболеваний малых дыхательных путей, уже продемонстрированная во многих исследованиях, может быть связана со способностью макролидов подавлять нейтрофильное воспаление . Принципиальным различием между терапией ГКС/иммуносупрессантами и макролидами является ингибирование различных митоген-активированных протеинкиназ, таких как р38-МАРК, экстрацеллюлярно регулируемой киназы и Janus-N-концевой киназы, а также уменьшение окислительного стресса макролидами, но не ГКС/иммуносупрессантами .
Возможным механизмом положительного влияния макролидов на воспалительный процесс при патологии дыхательных путей является их способность модулировать бактериальную вирулентность. Кроме того, макролиды способны уменьшить формирование биопленок .
Относительно недавно было опубликовано самое масштабное на сегодня исследование, посвященное изучению влияния длительной терапии азитромицином на развитие обострений ХОБЛ . В исследование было включено 1 142 больных ХОБЛ (средний OФB1 40 ± 16%), которые в течение 1-го года принимали либо азитромицин в дозе 250 мг/сут ежедневно (570 пациентов), либо плацебо (572 пациента). Число обострений ХОБЛ оказалось существенно ниже у больных, принимавших азитромицин: 741 против 900 в группе плацебо, т. е. риск развития обострений составил 0,73 (р < 0,001). Частота обострений на одного человека в год составила 1,48 и 1,83, а среднее время до следующего обострения - 266 против 174 дней (р < 0,001) соответственно в группах азитромицина и плацебо (рис.7). Не было отмечено различий между группами пациентов по числу госпитализаций в стационар, однако число незапланированных визитов оказалось меньше среди больных, принимавших азитромицин: 2,46 против 2,57 на одного пациента в год (р = 0,048).
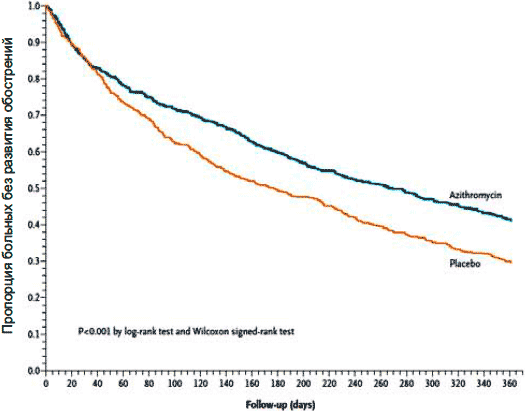
Рисунок 7.
Развитие обострений ХОБЛ при терапии азитромицином и плацебо (Alberts et al. N Engl J Med, 2011) обострений ХОБЛ . В исследование было включено
Несмотря на полученные обнадеживающие данные о возможности использования макролидов у больных с хроническими воспалительными заболеваниями легких, нельзя не обсудить проблему безопасности длительной терапии данными препаратами. Продолжительная терапия макролидами может привести к селекции штаммов микроорганизмов, резистентных к данному классу антибиотиков, что особенно актуально для S. pneumoniae . Кроме того, известны случаи, когда терапия макролидами приводила к развитию побочных явлений со стороны желудочно-кишечного тракта , кардиотоксичным (нарушение внутрисердечной проводимости) и ототоксичным эффектам .
Статины
Довольно неожиданно хорошо изученные «нереспираторные» препараты - статины (ингибиторы ГМГ-КоА-редуктазы) недавно привлекли внимание и с точки зрения терапии ХОБЛ. Статины обладают универсальными противовоспалительными эффектами, в т. ч. они способны уменьшить выраженность воспаления дыхательных путей, индуцированного табачным дымом . Статины уменьшают экспрессию поверхностных молекул адгезии на эндотелиальных клетках, макрофагах и эозинофилах, а также хемокиновых рецепторов, что приводит к снижению рекрутирования и миграции таких клеток воспаления, как нейтрофилы . Кроме того, статины подавляют продукцию провоспалительных цитокинов.
Согласно результатам когортных исследований статины могут уменьшить число обострений и летальность больных ХОБЛ . Также на фоне приема статинов отмечено уменьшение выраженности тяжести обострений, числа интубаций трахеи и потребности использования респираторной поддержки во время обострений . По данным двух исследований, статины способны замедлить прогрессирование ХОБЛ . Lee и колл. показали, что у пациентов с ХОБЛ на фоне приема статинов наблюдается снижение сывороточного уровня СРБ и повышение физической выносливости .
Антагонисты медиаторов
В формировании воспалительного ответа при ХОБЛ участвуют многие медиаторы , и антагонисты некоторых из них теоретически могут быть использованы для контроля воспаления у пациентов с ХОБЛ. Уже сегодня можно привести несколько примеров использования таких препаратов в пилотных исследованиях.
Фактор некроза опухоли (TNF-α) является универсальным цитокином, принимающим участие в хемотаксисе и активации макрофагов и нейтрофилов. Повышенные уровни TNF-a способствуют развитию апоптоза миоцитов поперечно-полосатых мышц и их атрофии . Rennard и колл. провели многоцентровое РКП, в котором изучали эффективность терапии инфликсимабом - человеческим моноклональным антителом к TNF-a - у пациентов с ХОБЛ . Препарат хорошо переносился пациентами, однако не снижал число обострений и не улучшал качество жизни больных. В данном исследовании была отмечена недостоверная тенденция к повышению числа опухолей и пневмоний на фоне приема инфликсимаба .
Цитокин IL-8 также играет большую роль в воспалительном каскаде, приводя к повышенной миграции и активации нейтрофилов . В единственном на сегодня РКП человеческий моноклональный IgG2 к IL-8 (ABX-IL8) назначали пациентам с ХОБЛ в виде 3 инфузий в течение 3 месяцев . По сравнению с плацебо терапия ABX-IL8 привела к статистически значимому улучшению одышки (по шкале Transitional Dyspnea Index), но не было различий по другим показателям эффективности (функциональные параметры, качество жизни и 6-минутный тест). Была отмечена хорошая переносимость препарата.
Лейкотриен В4 (LTB4), дериват арахидоновой кислоты, является хемоаттрактантом и активатором нейтрофилов . Эффективность ингибитора синтеза лейкотриенов BAYx1005 была изучена в небольшом исследовании II фазы у больных ХОБЛ . Терапия препаратом в течение 14 дней приводила к значительному снижению концентрации LTB4 в мокроте по сравнению с плацебо . Так как подавление синтеза лейкотриенов может быть важным методом влияния на нейтрофильное воспаление, обсуждается вопрос о проведении дальнейших исследований с подобными препаратами при ХОБЛ .
Заключение
Воспаление у «здоровых» курильщиков по составу клеточных элементов, медиаторов и протеаз очень похоже на воспаление у пациентов с ХОБЛ, но менее выражено. Поэтому полагают, что воспаление в дыхательных путях и паренхиме при ХОБЛ представляет собой усиленный хронический воспалительный ответ на ирританты (такие как табачный дым). К числу широко используемых противовоспалительных препаратов при ХОБЛ относятся ИГКС, как правило, в виде комбинаций с ДДБА. Новые перспективы противовоспалительной терапии ХОБЛ связывают с препаратами из класса ингибиторов фосфодиэстеразы-4 (рофлумиласт), с макролидами, статинами и новыми антагонистами медиаторов.
ЛИТЕРАТУРА
1. Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO workshop report. Last updated 2011.
2. Celli B.R., MacNee W. ATS/ERS Task Force. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004; 23: 932-946.
3. Buist A.S., McBurnie M.A., Vollmer W.M. et al. International variation in the prevalence of COPD (the BOLD Study): a population-based prevalence study. Lancet 2007; 370: 741-50.
4. Mannino D.M., Ноmа D.M., Akinbami L. et al. Chronic obstructive pulmonary disease surveillance - United States, 1971-2000. MMWR Surveill Summ 2002; 51: 1-16.
5. Murray C.J., Lopez A.D. Alternative projections of mortality and disability by cause 1990-2020: Global Burden of Disease Study. Lancet 1997; 349: 1498-504.
6. Barnes P.J., Shapiro S.D., Pauwels R.A. Chronic obstructive pulmonary disease: molecular and cellular mechanisms. Eur Respir J 2003; 22: 672-88.
7. HoggJ.C. Pathophysiology of airflow limitation in chronic obstructive pulmonary disease. Lancet 2004; 364: 709-21.
8. Barnes P.J. Chronic obstructive pulmonary disease. N Engl J Med 2000; 343: 269-80.
9. Barnes P.J. Molecular genetics of chronic obstructive pulmonary disease. Thorax 1999; 54: 245-52.
10. Meshi B., Vitalis T.Z., Ionescu D., Elliott W.M., Liu С., Wang X.D. et al. Emphysematous lung destruction by cigarette smoke. The effects of latent adenoviral infection on the lung inflammatory response. Am J Respir Cell Mol Biol 2002; 26: 52-7.
11. Ito K., Barnes PJ., Adcock I.M. Glucocorticoid receptor recruitment of histone deacetylase 2 inhibits interleukin- lb-induced histone H4 acetylation on lysines 8 and 12. Mol Cell Biol 2000; 20: 6891-903.
12. Hogg J.C., Macklem P.T., Thurlbeck W.M. Site and nature of airway obstruction in chronic obstructive lung disease. N Engl J Med 1968; 278: 1355-1360.
13. O’Donnell R.A., Peebles С., Ward J.A. et al. Relationship between peripheral airway dysfunction, airway obstruction, and neutrophilic inflammation in COPD. Thorax 2004; 59: 837-842.
14. Nadel J.A. Role of neutrophil elastase in hypersecretion during COPD exacerbations, and proposed therapies. Chest 2000; 117: Suppl. 2, 386S-389S.
15. Finkelstein R, Ma H.D., Ghezzo H. et al. Morphometry of small airways in smokers and its relationship to emphysema type and hyperresponsiveness. Am J Respir Crit Care Med 1995; 152: 267-276.
16. Frankenberger М., Menzel М., Betz R. et al. Characterization of a population of small macrophages in induced sputum of patients with chronic obstructive pulmonary disease and healthy volunteers. Clin Exp Immunol 2004; 138: 507-516.
17. Saetta М., Mariani М., Panina-Bordignon P. et al. Increased expression of the chemokine receptor CXCR3 and its ligand CXCL10 in peripheral airways of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2002; 165: 1404-1409.
18. Fairclough L„ Urbanowicz R.A., Corne J., et al. Killer cells in chronic obstructive pulmonary disease. Clin Sci (Lond) 2008; 114: 533-541.
19. Grashoff W.F., Sont J.K., Sterk P.J., et al. Chronic obstructive pulmonary disease: role of bronchiolar mast cells and macrophages. Am J Pathol 1997; 151: 1785-1790.
20. Saetta М., Di Stefano A., Maestrelli P., et al. Airway eosinophilia in chronic bronchitis during exacerbations. Am J Respir Crit Care Med 1994; 150: 1646-1652.
21. Papi A., Bellettato C.M., Braccioni F., et al. Infections and airway inflammation in chronic obstructive pulmonary disease severe exacerbations. Am J Respir Crit Care Med 2006; 173: 1114-1121.
22. Snoeck-Stroband JB, Lapperre TS, Gosman MM, et al. Chronic bronchitis sub-phenotype within COPD: inflammation in sputum and biopsies. Eur Respir J 2008; 31: 70-77.
23. Rutgers SR, Postma DS, ten Hacken NH, Kauffman HF, Der Mark TW, ter GH, et al. Ongoing airway inflammation in patients with COPD who do not currently smoke. Thorax 2000; 55: 12-18.
24. Antoniu S.A. New therapeutic options in the management of COPD - focus on roflumilast. Int J Chron Obstruct Pulmon Dis 2011; 6: 147-155.
25. Yamaya M, Azuma A, Takizawa H. Macrolide effects on the prevention of COPD exacerbations. Eur Respir J 2012; 40:485-494.
26. Young RP, Hopkins R, Eaton ТЕ. Pharmacological actions of statins: potential utility in COPD. Eur Respir Rev 2009; 18: 1-11.
27. Cazzola M, Dahl R. Inhaled combination therapy with long-acting β 2-agonists and corticosteroids in stable COPD. Chest 2004; 126: 220-237.

